مراجعة الفصل الرابع
املأ الفراغات بالكلمات المناسبة:
1. كل شيء يشغل حيزاً وله كتلة يسمى مادة.
2. الجسيمات الموجودة في نواة الذرة وتحمل شحنة موجبة وعددها يساوي العدد الذري تسمى بروتونات.
3. يوجد في نواة الذرة بروتونات ونيوترونات
4. عندما يرتبط عنصران أو أكثر كيميائياً فإن المادة الناتجة تسمى مركباً.
5. العناصر التي لها لمعان وموصلة للكهرباء والحرارة وقابلة للطرق والسحب وتشغل معظم الجدول الدوري هي الفلزات.
اختر الإجابة الصحيحة فيما يأتي:
6. يعد محلول السكر والماء:
أ. عنصراً.
ب. مخلوطاً غير متجانس.
ج. مركباً.
د. مخلوطاً متجانساً.
7. تحتوي ذرة على 12 بروتوناً و12 نيوتروناً وتحتوي ذرة أخرى على 12 بروتوناً و16 نيوتروناً وما هاتان الذرتان؟
أ. زرتا كروم.
ب. عنصران مختلفان.
ج. نظيران للعنصر نفسه.
د. مشحونتان شحنة سالبة.
8. إذا تماثلت العناصر المكونة لمركبين فلا بد أن:
أ. المركبين متماثلان.
ب. خصائص المركبين الفيزيائية والكيميائية متماثلة.
ج. الصيغ الكيميائية للمركبين متماثلة.
د. الرموز الكيميائية في صيغ المركبين متماثلة لكن الأرقام قد تختلف.
9. تتكون الذرة من:
أ. إلكترونات وبروتونات.
ب. نيوترونات وبروتونات.
ج. إلكترونات وبروتونات ونيوترونات.
د. عناصر وبروتونات وإلكترونات.
10. الجسيمات ذات الشحنة السالبة في الذرة هي:
أ. البروتونات.
ب. الإلكترونات.
ج. النيوترونات.
د. النواة.
11. أين تتواجد الإلكترونات في الذرة؟
أ. في النواة مع البروتونات.
ب. مرافقة للنيوترونات.
ج. حول النواة على شكل سحابة إلكترونية.
د. في الجدول الدوري للعناصر.
12. أي المواد التالية خليط غير متجانس؟
أ. الهواء.
ب. السلطة.
ج. عصير التفاح.
د. سبيكة الذهب.
13. صف استخدام الجدول الدوري لإيجاد العدد الذري لكل من الكربون والصوديوم والنيكل.
C=6, Na=11, Ni= 28
14. ما العنصر الذي يحتوي على 7 بروتونات؟
الذرة التي تحتوي على سبع بروتونات هي النيتروجين.
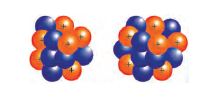
15. الرسمان التاليان لذرتي كربون ما هل هما نظيران أم لا؟ فسر إجابتك
الذرتان نظيران لأنهما تتساويان في عدد البروتونات وتختلفان في عدد النيوترونات وإحدى الذرتين تحتوي على (6) بروتونات و(6) نيوترونات بينما تحتوي الأخرى على (6) بروتونات و(8) نيوترونات.
16. فسر كيف يمكن ان يكون (كوبالت - 60) و(كوبالت - 59) العنصر نفسه مع أن لكل منهما عدداً كتلياً مختلفاً.
الكوبلت -60 والكوبلت -59 نظيران لأن كلاً منهما يحوي على (27) بروتوناً في نواته.
17. اشرح كيف يمكن حساب الكتلة الذرية للعنصر؟
تتحدد الكتلة لذرية للعنصر باستخدام متوسط كتل نظائر العنصر.
18. اعمل بحثاً تخيل نفسك صحفياً في العام 1896 م وقد سمعت عن اكتشاف الإلكترون اعمل بحثاً واكتب مقالة تتكلم فيها عن اكتشاف الإلكترون والعالم الذي اكتشفه.
معلومات عن العالم تومسون واكتشافاته من خلال تجربة أنابيب التفريغ الكهربائي وتجربة أنبوب أشعة الكاثود.
19. الكتلة الذرية عنصر الكربيتون له ستة نظائر طبيعية أعدادها الكتلية: 78 , 80 , 82, 83, 84 , 86
اعمل جدولاً بين عدد البروتونات والإلكترونات والنيوترونات في كل من تلك النظائر.
| النظير | بروتون | إلكترون | نيوترون |
| Kr-78 | 36 | 36 | 42 |
| Kr-80 | 36 | 36 | 44 |
| Kr-82 | 36 | 36 | 46 |
| Kr-83 | 36 | 36 | 47 |
| Kr-84 | 36 | 36 | 48 |
| Kr-86 | 36 | 36 | 50 |
20. نسبة الذرات ما نسبة الهيدروجين إلى الأوكسجين في كل من حمض الكبريتيك (H2SO4) وفوق أكسيد الهيدروجين (H2O2)؟
1:1, 2:1. 20


.JPG)
.JPG)
.JPG)
.JPG)
.JPG)